目次
活性化過電圧とは
燃料電池では、理論電圧(おおよそ1.23 V)よりも実際の電圧が低くなります。 その主な要因のひとつが活性化過電圧(ηact)です。
これは、電極での電気化学反応を進めるために必要な余分の電位差で、特に低電流密度領域で支配的になります。
活性化過電圧の式(ターフェル式)
活性化過電圧は、電流密度 i に対してターフェル式(Tafel equation)で近似されます。
ηact = a + b log i
- a:切片(交換電流密度や電極状態に依存)
- b:ターフェル勾配(反応の速度論的パラメータ、電子数 n、移動係数 α などで決まる)
この式から分かるように、ηact は電流密度の対数に比例して増加し、低電流域で支配的に現れます。
測定方法
(1) 内部抵抗の補正(IR補正)
実験的に得られる電池の電圧には、抵抗過電圧(IR drop)が重なっています。 そのため、まずは交流インピーダンス測定器や高周波抵抗計を用いて内部抵抗 R を測定し、
VIR-free = Vcell + iR
として補正します。これにより純粋な過電圧成分を抽出できます。
(2) 低電流密度領域での近似
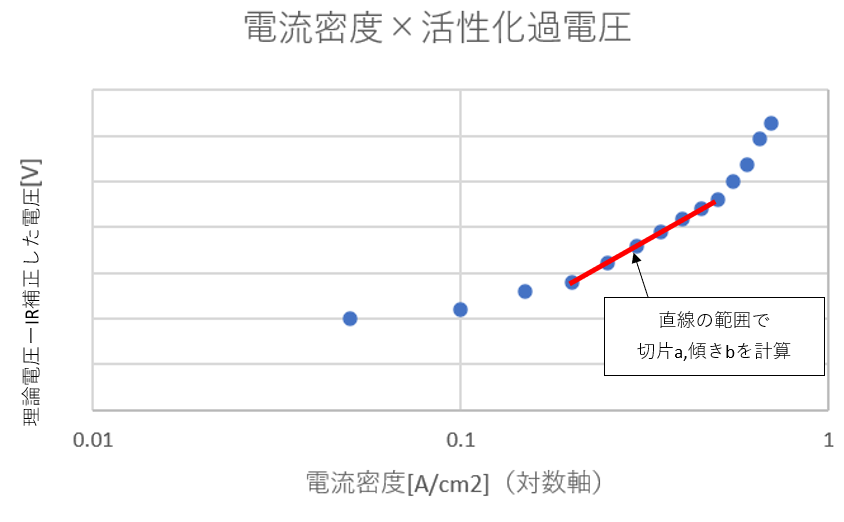
IR補正した電圧から、理論電圧(通常1.23V程度)との差を活性化過電圧とみなします。 電流密度と ηact の関係を片対数プロット(η vs log i)すると直線関係が得られます。
この直線(下図赤線)をフィッティングして、切片 a、傾き b を求めます。
実務での意味
- 切片 a:電極触媒の性能や電極表面状態に依存するため、触媒の改良や劣化評価に利用されます。
- 傾き b:反応機構や電子移動係数 α に関係するため、基礎研究では反応機構解明に役立ちます。
まとめ
- 活性化過電圧は燃料電池の低電流域での性能低下を支配する要因。
- IR補正を行った後に、ターフェル式 η = a + b log i を用いて解析する。
- a, b の値を調べることで、触媒性能や反応機構を評価できる。
👉 本記事では活性化過電圧に絞って解説しました。
濃度過電圧については別記事で詳しく扱う予定です。
